
|
Trabajo catalogado en |
Síntesis: Generalidades sobre pilas y baterías.Realizado por: Damián Bragonzi, Nicolás Gómez y Cristian Toledo, E.E.T. Nro. 4 de Vicente López. Tamaño: 204 KB. Fecha de Publicación/Corrección: Diciembre de 2001. |

Pila eléctrica:
Dispositivo que convierte la energía química en eléctrica. Todas las pilas consisten en un electrólito (que puede ser líquido, sólido o en pasta), un electrodo positivo y un electrodo negativo. El electrólito es un conductor iónico; uno de los electrodos produce electrones y el otro electrodo los recibe. Al conectar los electrodos al circuito que hay que alimentar, se produce una corriente eléctrica.
Las pilas en las que el producto químico no puede volver a su forma original una vez que la energía química se ha transformado en energía eléctrica (es decir, cuando las pilas se han descargado), se llaman pilas primarias o voltaicas. Las pilas secundarias o acumuladores son aquellas pilas reversibles en las que el producto químico que al reaccionar en los electrodos produce energía eléctrica, puede ser reconstituido pasando una corriente eléctrica a través de él en sentido opuesto a la operación normal de la pila.

Pilas Primarias:
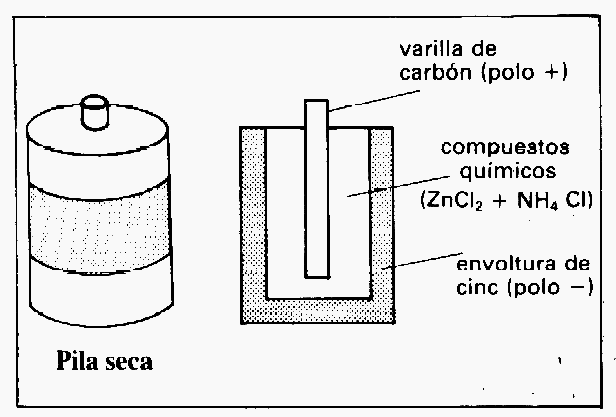
La pila primaria más común es la pila Leclanché o pila seca, inventada por el químico francés Georges Leclanché en la década de 1860. La pila seca que se utiliza hoy es muy similar al invento original. El electrólito es una pasta consistente en una mezcla de cloruro de amonio y cloruro de cinc. El electrodo negativo es de cinc, igual que el recipiente de la pila, y el electrodo positivo es una varilla de carbono rodeada por una mezcla de carbono y dióxido de manganeso. Esta pila produce una fuerza electromotriz de unos 1,5 voltios.
Este tipo de pila se utiliza frecuentemente en aparatos de radio, calculadoras, etcétera, en los que suelen ir asociadas en serie.
Cuando los compuestos químicos iniciales de una pila seca se han agotado y transformado en otros, se dice que la pila está descargada y hay que desecharla.
Otra pila primaria muy utilizada es la pila de cinc-óxido de mercurio, conocida normalmente como batería de mercurio. Puede tener forma de disco pequeño y se utiliza en audífonos, células fotoeléctricas y relojes de pulsera eléctricos. El electrodo negativo es de cinc, el electrodo positivo de óxido de mercurio y el electrólito es una disolución de hidróxido de potasio. La batería de mercurio produce 1,34 V, aproximadamente.
La pila de combustible es otro tipo de pila primaria. Se diferencia de las demás en que los productos químicos no están dentro de la pila, sino que se suministran desde fuera.
Pilas secundarias:
El acumulador o pila secundaria, que puede recargarse invirtiendo la reacción química, fue inventado en 1859 por el físico francés Gastón Planté. La pila de Planté era una batería de plomo y ácido, y es la que más se utiliza en la actualidad. Esta batería, que contiene de tres a seis pilas conectadas en serie, se usa en automóviles, camiones, aviones y otros vehículos. Su ventaja principal es que puede producir una corriente eléctrica suficiente para arrancar un motor; sin embargo, se agota rápidamente. El electrólito es una disolución diluida de ácido sulfúrico, el electrodo negativo es de plomo y el electrodo positivo de dióxido de plomo. En funcionamiento, el electrodo negativo de plomo se disocia en electrones libres e iones positivos de plomo. Los electrones se mueven por el circuito eléctrico externo y los iones positivos de plomo reaccionan con los iones sulfato del electrólito para formar sulfato de plomo. Cuando los electrones vuelven a entrar en la pila por el electrodo positivo de dióxido de plomo, se produce otra reacción química. El dióxido de plomo reacciona con los iones hidrógeno del electrólito y con los electrones formando agua e iones plomo; estos últimos se liberarán en el electrólito produciendo nuevamente sulfato de plomo.
Un acumulador de plomo y ácido se agota porque el ácido sulfúrico se transforma gradualmente en agua y en sulfato de plomo. Al recargar la pila, las reacciones químicas descritas anteriormente se invierten hasta que los productos químicos vuelven a su condición original. Una batería de plomo y ácido tiene una vida útil de unos cuatro años. Produce unos 2 V por pila. Recientemente, se han desarrollado baterías de plomo para aplicaciones especiales con una vida útil de 50 a 70 años.

Acumulador de plomo
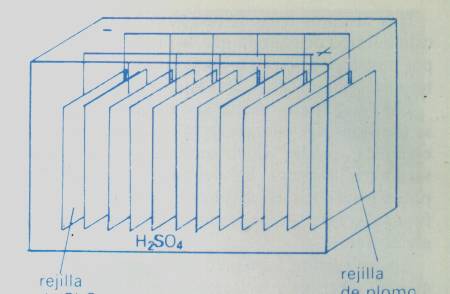
Interior del Acumulador de plomo
Otra pila secundaria muy utilizada es la pila alcalina o batería de níquel y hierro, ideada por el inventor estadounidense Thomas Edison en torno a 1900. El principio de funcionamiento es el mismo que en la pila de ácido y plomo, pero aquí el electrodo negativo es de hierro, el electrodo positivo es de óxido de níquel y el electrólito es una disolución de hidróxido de potasio. La pila de níquel y hierro tiene la desventaja de desprender gas hidrógeno durante la carga. Esta batería se usa principalmente en la industria pesada. La batería de Edison tiene una vida útil de unos diez años y produce 1,15 V, aproximadamente.
Otra pila alcalina similar a la batería de Edison es la pila de níquel y cadmio o batería de cadmio, en la que el electrodo de hierro se sustituye por uno de cadmio. Produce también 1,15 V y su vida útil es de unos 25 años.
Pilas Solares:
Las pilas solares producen electricidad por un proceso de conversión fotoeléctrica. La fuente de electricidad es una sustancia semiconductora fotosensible, como un cristal de silicio al que se le han añadido impurezas. Cuando la luz incide contra el cristal, los electrones se liberan de la superficie de éste y se dirigen a la superficie opuesta. Allí se recogen como corriente eléctrica. Las pilas solares tienen una vida muy larga y se utilizan sobre todo en los aviones, como fuente de electricidad para el equipo de a bordo.
Pila de combustible
:Mecanismo electroquímico en el cual la energía de una reacción química se convierte directamente en electricidad. A diferencia de la pila eléctrica o batería, una pila de combustible no se acaba ni necesita ser recargada; funciona mientras el combustible y el oxidante le sean suministrados desde fuera de la pila.
Una pila de combustible consiste en un ánodo en el que se inyecta el combustible -comúnmente hidrógeno, amoníaco o hidracina- y un cátodo en el que se introduce un oxidante -normalmente aire u oxígeno. Los dos electrodos de una pila de combustible están separados por un electrólito iónico conductor. En el caso de una pila de combustible de hidrógeno-oxígeno con un electrólito de hidróxido de metal alcalino, la reacción del ánodo es 2H2 + 4OH- → 4H 2O + 4e- y la reacción del cátodo es O2 + 2H2O + 4e- → 4OH-. Los electrones generados en el ánodo se mueven por un circuito externo que contiene la carga y pasan al cátodo. Los iones OH- generados en el cátodo son conducidos por el electrólito al ánodo, donde se combinan con el hidrógeno y forman agua. El voltaje de la pila de combustible en este caso es de unos 1,2 V pero disminuye conforme aumenta la carga. El agua producida en el ánodo debe ser extraída continuamente para evitar que inunde la pila. Las pilas de combustible de hidrógeno-oxígeno que utilizan membranas de intercambio iónico o electrólitos de ácido fosfórico fueron utilizados en los programas espaciales Gemini y Apolo respectivamente. Las de ácido fosfórico tienen un uso limitado en las instalaciones eléctricas generadoras de energía.

Actualmente se están desarrollando las pilas de combustible con electrólitos de carbonato fundido. El electrólito es sólido a temperatura ambiente, pero a la temperatura de operación (650 a 800 °C), es un líquido con iones carbonato conductores. Este sistema tiene la ventaja de utilizar monóxido de carbono como combustible, por lo que pueden utilizarse como combustible mezclas de monóxido de carbono e hidrógeno como las que se producen en un gasificador de carbón.
También se están desarrollando pilas de combustible que emplean dióxido de circonio sólido como electrólito. Estas pilas se llaman pilas de combustible de óxido sólido. El dióxido de circonio se convierte en un conductor iónico a unos 1.000 °C. Los combustibles más adecuados son el hidrógeno, el monóxido de carbono y el metano, y al cátodo se le suministra aire u oxígeno. La elevada temperatura de operación de las pilas de combustible de óxido sólido permite el uso directo de metano, un combustible que no requiere catalizadores costosos de platino sobre el ánodo. Las pilas de combustible de óxido sólido tienen la ventaja de ser relativamente insensibles a los contaminantes del combustible, como los compuestos de azufre y nitrógeno que empeoran el rendimiento de otros sistemas de combustible.
La temperatura relativamente elevada de operación de las pilas de combustible de carbonato fundido y óxido sólido facilitan la eliminación en forma de vapor del agua producida por la reacción. En las pilas de combustible de baja temperatura se deben tomar medidas para eliminar el agua líquida de la cámara del ánodo.
Baterías:
Aparato que transforma la energía química en eléctrica, y consiste en dos o más pilas eléctricas conectadas en serie o en paralelo en mixto. Se han desarrollado diversos tipos de nuevas baterías para vehículos eléctricos. Se trata de versiones mejoradas de las baterías convencionales, pero aún tienen numerosos inconvenientes como su corta duración, alto costo, gran volumen o problemas medioambientales. Las baterías destinadas a vehículos eléctricos incorporan sulfuro de litio-hierro, cinc-cloro, hidruro de níquel y sulfuro de sodio. Las compañías suministradoras de electricidad están desarrollando este tipo de baterías para utilizarlas como "niveladores de carga", a fin de compensar las fluctuaciones esporádicas del sistema. Estas baterías ocupan poco espacio y apenas tienen efectos dañinos para el medioambiente.

La batería para automóviles que se puede adquirir en cualquier almacén de repuestos produce energía gracias a que contiene una solución acuosa de ácido sulfúrico conocida como electrolitos líquidos.
Los electrolitos, en las baterías, al entrar en contacto con una lámina de metal, usualmente de plomo y conocida como electrodo, produce reacciones químicas que liberan energía, la cual es trasmitida por el mismo electrodo.

La energía química, en este caso, es producto del intercambio de iones que conforman la solución acuosa o electrolitos y de los electrones de los átomos de la lámina de metal o electrodo. Los iones son átomos a los que les falta o les sobra por lo menos un electrón.
El intercambio de iones también se presenta en los sistemas biológicos. Al igual que en las pilas, en los seres vivos esta reacción química también libera energía, la cual nos permite pensar, mover el cuerpo o desplazarnos de un lugar a otro
Uno de los grandes inconvenientes de las reacciones químicas en las baterías radica en que mientras liberan energía los electrolitos y electrodos se transforman en gases contaminantes, ácido sulfuroso y otros desechos.
Las baterías al igual que en las pilas comunes y corrientes, poseen celdas que generan hasta 1,5 voltios, de tal suerte que del número de celdas depende el tamaño y la potencia requerida.
Posteriormente se desarrolló un material de electrolito sólido con base en el pegante conocido como Colbón de la firma BASF, que se encuentra en cualquier tienda o supermercado.

El Colbón se lava con agua, se deja evaporar hasta que queda una membrana del grosor de una hoja de papel y luego de un proceso de mezclas con otras sales y ácidos queda convertido en una fina capa con capacidad para generar energía, casi tan eficiente como la solución acuosa que usan las pilas que se encuentran en el mercado. Con este nuevo material se utilizaron diferentes electrodos o conductores de energía, tales como láminas de carbono, plata y acero inoxidable. Como resultado, el nuevo material generó un voltio de energía por celda, mientras que una pila o una batería normal con electrolitos líquidos produce hasta 1,5 voltios por celda.
Por ahora, muchos científicos en sus laboratorios, especialmente en países desarrollados, buscan afanosamente encontrar un electrolito en estado sólido que genere 1,2 voltios o más por celda. De lograrlo se podrán mejorar la calidad de las pilas y las baterías para que no contaminen, prolonguen su duración y, como si fuera poco, la posibilidad de reducir su tamaño permitirá a la ciencia incluir diminutas pilas, de larga duración, en tarjetas electrónicas inteligentes que le darían un gigantesco impulso al desarrollo tecnológico en todo el planeta.

-Enciclopedia Microsoft Encarta 2000
-Enciclopedia Larousse Edición 1995.
-www.cienciaaldia.com
-Enciclopedia Océano Edición 1997.
-Física 1 Santillana polimodal.